 Blog HemoClass
Blog HemoClass
 TAG: #Padronização
TAG: #Padronização
png.jpg)
Linfócito reativo em crianças: por que é um achado normal (e como interpretar sem pânico)
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
21/10/2025 |
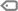 #Leucograma
#Padronização
#Hematoscopia
#exames
#Leucograma
#Padronização
#Hematoscopia
#exames
O que é um linfócito reativo?
É um linfócito que “ganhou corpo” após ativação antígeno–anticorpo. Essa ativação leva a alterações morfológicas (citoplasma mais amplo e basofílico, contorno irregular, às vezes nucléolo evidente) e funcionais (produção de anticorpos, citocinas etc.). Em outras palavras: é o linfócito fazendo o seu trabalho.
Por que aparecem tanto em crianças?
Exposição constante a antígenos novos: cada vacina, infecção banal e contato ambiental apresenta “novos cartões de visita” ao sistema imune.
Maturação imunológica acelerada: nos primeiros anos, há uma verdadeira “academia” para linfócitos B e T.
Janela etária típica: do nascimento até ~3,5–4 anos, é comum ver LR no esfregaço.
Resumo prático: em pediatria, encontrar LR é normal e esperado. Um hemograma de uma criança de ~2 anos completamente “estéreo” de LR pode, inclusive, levantar sobrancelhas — sempre dentro do contexto clínico.
Como interpretar no hemograma
1) Não olhar só para a contagem total
LR podem aparecer com leucócitos normais. “Só libero LR quando há leucocitose” é um erro. Contexto é rei: quadro clínico, diferencial leucocitário, morfologia.
2) Valor absoluto vs. percentual
Relate percentual e, quando possível, o valor absoluto. Pequenos percentuais em amostras com linfocitose típica da infância ainda são condizentes com fisiologia.
3) Descrição morfológica ajuda o clínico
Se o laboratório utiliza microscopia, vale caracterizar brevemente (p. ex.: “linfócitos com citoplasma basofílico amplo, contorno irregular, compatíveis com reatividade”). Evite termos alarmistas.
Quando o LR não é só fisiologia? (sinais de alerta)
Embora raro, há contextos que pedem atenção e correlação clínica:
Citopenias associadas (anemia, trombocitopenia relevantes)
Aparência atípica não compatível com reatividade usual (suspeita de blastos)
Sintomas sistêmicos importantes (perda ponderal, febre prolongada, sangramentos, linfonodomegalias exuberantes)
Padrões persistentes e desproporcionais sem explicação clínica (ex.: LR altos por longos períodos, fora de infecções/vacinas)
Nesses cenários, o caminho é discutir com o pediatra, considerar repetição do exame, revisão do esfregaço e, se indicado, investigação direcionada.
Erros comuns (e como evitá-los)
Nunca “liberar” LR em crianças
Errado. Em crianças pequenas, LR são comuns. Omiti-los prejudica a leitura do caso.
Só “liberar” LR quando há leucocitose
Errado. LR podem aparecer com leucócitos normais. O achado é morfológico/funcional, não depende da contagem total.
Laudo genérico, sem contexto
Melhor: incluir observações curtas e úteis (“achado compatível com faixa etária/reatividade imunológica”, “correlacionar com quadro clínico”).
Boas práticas para laboratórios e profissionais
Padronize critérios de identificação e relato de LR (checklists morfológicos ajudam).
Comunique “sem drama”: use linguagem clara e educativa no comentário do laudo.
Integre com a clínica: se houver sinal de alerta, destaque e sugira correlação/seguimento.
Eduque pais/cuidadores: quando houver contato direto, explique que LR é, na maioria, “sinal de defesa”, não de gravidade.
Exemplo de comentário de laudo (sugestão):
“Presença de linfócitos reativos, achado comum na faixa etária pediátrica e compatível com resposta imune. Correlacionar com quadro clínico. Sem outras atipias relevantes no esfregaço.”
Para pais e cuidadores: uma explicação simples
“Linfócito reativo” significa que células de defesa do seu filho foram ativadas — geralmente por contato com vírus, bactérias, vacinas ou outros estímulos normais nesta fase da vida. Na grande maioria dos casos, não é motivo de pânico. O médico avalia o resultado junto com os sintomas e com o restante do exame.
Perguntas frequentes (FAQ)
1) LR é sinal de infecção grave?
Na maioria das vezes, não. É um marcador de resposta imune, comum em resfriados, pós-vacina e outras exposições benignas.
2) Precisa repetir o hemograma por causa de LR?
Depende do contexto. Se a criança está bem e o restante do hemograma está ok, geralmente não.
3) LR vira “câncer de sangue”?
LR não são blastos. São células maduras ativadas. Preocupações com hematopatias surgem por conjunto de achados (morfologia suspeita, citopenias, clínica), não por LR isolado.
4) Existe “valor normal” de LR?
Relata-se presença e percentual; não há um “valor de referência” universal — o importante é a interpretação contextual (idade, clínica, demais parâmetros).
Principais aprendizados
Em crianças (RN → ~4 anos), linfócito reativo = achado esperado.
Não condicione o relato de LR à presença de leucocitose.
Descreva e contextualize: ajuda o pediatra e evita alarmes desnecessários.
Fique atento aos sinais de alerta para diferenciar reatividade fisiológica de situações que pedem investigação.
No HemoClass LAN você entenderá DEFINITIVAMENTE as alterações hematológicas com base na fisiopatologia de cada alteração/processo.
O LAN é disparado a MELHOR FORMAÇÃO em hematologia do mercado!

Alterações Hematológicas no Uso Crônico de Álcool: Causas, Diagnóstico e Apoio Laboratorial
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
11/08/2025 |
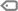 #Padronização
#Sindromes
#exames
#Padronização
#Sindromes
#exames
Alterações Hematológicas no Uso Crônico de Álcool: Como Identificar e Interpretar no Laboratório
Na rotina de um laboratório clínico, não é incomum receber hemogramas com alterações que, à primeira vista, parecem não ter explicação. Trombocitopenia repentina, pancitopenia sem causa aparente, anemias incomuns — tudo isso pode levantar dúvidas e atrasar a liberação de resultados.
Em muitos desses casos, um fator comum aparece quando investigamos mais a fundo: o uso crônico de álcool.
Por que o uso crônico de álcool altera o hemograma?
O etanol exerce múltiplos efeitos nocivos sobre o sistema hematológico, e compreender esses mecanismos é essencial para evitar erros interpretativos:
Toxicidade medular: o álcool afeta diretamente a medula óssea, reduzindo a produção de eritrócitos, leucócitos e plaquetas, levando à pancitopenia periférica.
Deficiências nutricionais: compromete a absorção de vitaminas essenciais à hematopoese. A falta de vitamina B12 e ácido fólico causa anemia megaloblástica, enquanto a deficiência de vitamina B6 leva à anemia sideroblástica.
Síndrome de Zieve: caracterizada por anemia hemolítica, icterícia e hiperlipidemia, geralmente associada à deficiência de vitamina E e alterações na membrana eritrocitária.
Trombocitopenia alcoólica: pode ocorrer pela redução da trombopoietina hepática ou pelo hiperesplenismo decorrente de hipertensão portal em hepatopatias alcoólicas.
Apoptose plaquetária: o álcool pode induzir morte celular precoce nas plaquetas, aumentando o risco de sangramento.
Imunidade comprometida: o uso crônico prejudica a função de neutrófilos e macrófagos, elevando a suscetibilidade a infecções.
A importância da interpretação correta no laboratório
Nem sempre o prontuário do paciente traz informações claras sobre histórico de etilismo. Muitas vezes, o analista clínico precisa suspeitar do uso crônico de álcool a partir dos padrões hematológicos observados e buscar exames complementares para confirmar.
Uma interpretação segura depende de:
Correlação entre achados hematológicos e bioquímicos;
Conhecimento atualizado sobre mecanismos fisiopatológicos;
Atenção aos sinais indiretos no hemograma.
Quando buscar apoio especializado?
Casos complexos exigem decisões rápidas e embasadas. Ter acesso a uma assessoria remota em hematologia significa contar com suporte técnico imediato para discutir resultados, orientar investigações adicionais e padronizar laudos.
Esse suporte é especialmente valioso quando:
O hemograma apresenta alterações múltiplas e atípicas;
Há suspeita de condições como Síndrome de Zieve ou anemia sideroblástica;
O histórico clínico é incompleto ou inexistente.
Com esse tipo de parceria, o laboratório aumenta sua assertividade, reduz erros interpretativos e entrega mais valor para médicos e pacientes.
📌 Sua equipe pode interpretar hemogramas complexos com muito mais segurança. Conheça como nossa assessoria remota pode integrar conhecimento técnico-laboratorial à sua rotina e elevar a qualidade dos seus resultados.
Nos contate clicando AQUI para saber mais sobre o serviço de assessoria remota!
Texto produzido por Flavio Simplicio Maia - Assessor HemoClass
png.jpg)
5 Erros Fatais dos Analistas Clínicos O Último Pode Custar a Vida do Paciente!
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
20/01/2025 |
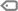 #Leucograma
#Padronização
#Hematoscopia
#exames
#HemoClass Leucemias
#Leucograma
#Padronização
#Hematoscopia
#exames
#HemoClass Leucemias
Aqui estão os 5 erros mais comuns que analistas clínicos cometem. O último é o mais perigoso de todos.
## **1) Não contar macroplaquetas de acordo com a recomendação** 🧐
As macroplaquetas são grandonas, chamam atenção na lâmina, mas será que você está liberando corretamente? Existe um limite tolerável para serem consideradas normais, e passar desse limite pode indicar uma alteração importante.
A ICSH (International Council for Standardization in Haematology) tem recomendações para esse tipo de contagem. Se você ignora essas diretrizes, pode estar colocando o paciente em risco.
🔎 **Lição:** Não é só contar e seguir a vida, é contar **certo**!
## **2) Não analisar a série vermelha** ❌🔬
Quem nunca ouviu aquela história do analista que só tem olhos para leucócitos e plaquetas? Pois é, essa fixação pode ser um problemão.
A série vermelha revela informações valiosas sobre anemias, distúrbios hematológicos e outras alterações clínicas. Se você não presta atenção nela, pode deixar passar um diagnóstico importante.
📌 **Exemplo:** Um paciente com hemólise pode ter alterações nas hemácias que dariam pistas valiosas, mas se você não olha para isso… bom, perdeu-se a chance de um diagnóstico precoce!
## **3) Confundir linfócito reativo (LR) com monócito** 🤯
Se eu ganhasse um real para cada vez que um iniciante confundiu LR com monócito, estaria escrevendo este texto direto de uma ilha paradisíaca.
Esse erro é clássico e gravíssimo. O linfócito reativo pode indicar infecções virais ou outros processos importantes. Se você confunde com um monócito, simplesmente **deleta um possível diagnóstico**.
🚨 **Dica de ouro:** LR tem citoplasma mais amplo, bordas irregulares e um comportamento bem diferente na lâmina. Treine seu olho para diferenciá-los!
## **4) Achar que todo hemograma tem pelo menos um bastonete** 🤦♂️
Essa é uma das maiores bobagens que circulam por aí. **Quem espalha essa "dica" simplesmente não entende hematologia!**
O bastonete aparece em resposta a infecções bacterianas, processos inflamatórios e algumas condições específicas. Mas dizer que **"todo hemograma tem que ter pelo menos um"**? Balela!
📢 **Regra real da hematologia:** Bastonete não é figurinha carimbada. Se ele está lá, é porque o organismo está reagindo a alguma coisa.
## **5) Contar blasto como célula imatura** 🚨⚠️
Esse é o erro mais grave da lista. Se tem um erro que pode **custar a vida do paciente**, é esse.
Blastos são **células malignas até que se prove o contrário**. Contar um blasto como "célula imatura genérica" pode atrasar um diagnóstico de leucemia, uma doença que precisa ser detectada rapidamente para que o tratamento tenha sucesso.
🔴 **Se você não conta blastos corretamente, o paciente pode pagar com a vida. Simples assim.**
---
## **E agora? Como evitar esses erros?**
A verdade é que a hematologia **não perdoa descuidos**. Se você quer evitar esses e outros erros que podem comprometer um diagnóstico, precisa investir no seu conhecimento.
👉 **A solução?** Seguir a **HemoClass**!
Lá dentro, você aprende a identificar **cada detalhe** na lâmina com segurança, confiança e precisão. Nada de achismos. Nada de dúvidas. Apenas análises certeiras e diagnósticos impecáveis.
🔬 **Quer se tornar um analista clínico diferenciado? Então não perca as publicacões aqui do nosso Super-Hemato-Blog🚀
png.jpg)
Descomplicando a Hematologia com a Metodologia 3R
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
08/01/2025 |
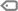 #Padronização
#Hematoscopia
#Consultoria
#Padronização
#Hematoscopia
#Consultoria
Se você já travou na frente do microscópio tentando entender uma alteração hematológica, saiba que não está sozinho. E se eu te contar que, muitas vezes, a culpa não é sua, mas do método que te ensinaram – ou da falta de método, para ser mais direto?
**Seja bem-vindo ao mundo da Hematologia real!**
Aqui, a gente deixa os mitos e regrinhas sem fundamento de lado e foca no que realmente importa: a ciência por trás da célula e a aplicação prática do conhecimento. Eu sou Paulo Merísio, professor de Hematologia há mais de 20 anos, palestrante em congressos no Brasil e no exterior, e criador da **Metodologia 3R**, que vai transformar sua forma de analisar e interpretar alterações hematológicas.
O que é a Metodologia 3R?
A Metodologia 3R é simples, mas poderosa. Ela se baseia em três pilares essenciais para qualquer profissional que deseja se destacar na área de Hematologia:
1. **Reconhecer**: Entenda os padrões celulares.
2. **Relatar**: Aprenda a descrever corretamente.
3. **Relacionar**: Conecte os achados laboratoriais com a clínica do paciente.
Agora, vamos detalhar cada um desses pilares de forma prática (e sem blá-blá-blá acadêmico).
---
Pilar 1: Reconhecer
"Monócito tem forma de rim", "Blasto tem nucléolo"... Quem nunca ouviu essas frases na faculdade? Spoiler: **muitas delas não funcionam na prática!** Para reconhecer uma alteração hematológica de verdade, você precisa observar o **padrão celular**, ou seja, aquilo que nunca muda em uma célula.
Por exemplo:
- **Drepanócito**: É uma célula com terminação em ponta e densidade aumentada por conta da hemoglobina polimerizada. Se não tem esses padrões, **não é um drepanócito**.
- **Linfócito reativo**: O tamanho ou o formato pouco importam. O padrão está na cromatina heterogênea e na basofilia citoplasmática. Simples assim.
Sem conhecer esses padrões, você corre o risco de identificar células de forma errada – e ninguém quer liberar um hemograma equivocado, né?
---
Pilar 2: Relatar
Imagine o seguinte cenário: você identificou um blasto no hemograma. E aí escreve no laudo: “presença de célula imatura”. **Pausa dramática.** Isso está completamente errado!
O médico não olha a lâmina; ele confia no que você escreve. Se o relato não segue as recomendações adequadas, o resultado perde credibilidade. Aqui vão algumas dicas práticas:
- **Blasto**: Deve ser contado e relatado como tal.
- **Eritroblastos**: Informe a proporção correta (X eritroblastos por 100 células nucleadas).
- **Linfócitos reativos**: Inclua-os na contagem diferencial.
Relatar corretamente não só evita confusões, mas também destaca seu trabalho no laboratório. Quando o médico consegue correlacionar o hemograma com a clínica do paciente de forma precisa, ele sabe quem está por trás daquele resultado impecável.
---
Pilar 3: Relacionar
Este é o grande diferencial dos especialistas em Hematologia. Reconhecer e relatar são importantes, mas entender **o que a alteração significa na clínica do paciente** é o que te coloca em outro nível.
Por exemplo:
- **Vacúolos no citoplasma de neutrófilos**: Sabia que eles podem indicar septicemia? Mas se a lâmina foi feita muito tempo após a coleta, esses vacúolos podem ser induzidos pelo EDTA. Entender a fisiologia é crucial para não cair em armadilhas.
Além disso, médicos frequentemente ligam pedindo explicações sobre alterações. Se você não souber responder, sua credibilidade (e a do laboratório) vai por água abaixo. Por outro lado, se você entende a fisiologia e sabe contextualizar a alteração, ganha destaque como profissional.
---
Por que a Metodologia 3R é essencial?
A Hematologia não é uma ciência "apertar botão". É um trabalho artesanal que exige conhecimento profundo e aplicação prática. É exatamente por isso que bons hematologistas são tão valorizados no mercado.
Se você quer se destacar, comece aplicando a Metodologia 3R na sua rotina. E se quiser dar um passo além, conheça meu curso **Hematologia Prática**, onde ensino como aplicar essa metodologia em todos os tipos de alterações hematológicas – de células vermelhas a blastos.
Para conhecer o curso hematologia prática clique AQUI
Gostou do conteúdo?
Compartilhe com seus colegas e não esqueça de se inscrever aqui no meu blog para continuar aprendendo Hematologia de verdade.
Nos vemos no próximo post! 😉
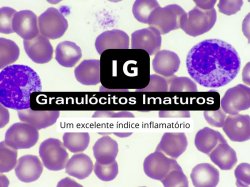
IG - Granulócitos Imaturos - Um Excelente Marcador Inflamatório
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
21/12/2023 |
 #Leucograma
#Padronização
#exames
#Leucograma
#Padronização
#exames
Alguns equipamentos automatizados liberam o índice IG - que significa granulócitos imaturos. Alguns ainda quantificam esse índice.
Mas o que é isso?
Ele é composto pela soma dos promielócitos, mielócitos e metamielócitos, com alta confiabilidade, ou seja, o IG precisa bater com a sua diferencial dessas células.
Muito se fala sobre a substituição do bastonete por esse índice, entretanto a contagem de bastonetes (diferencial manual) ainda é mais precoce em situações de inflamação aguda.
Quanto ao valor de referência é 0. Sim, em pacientes normais não se encontra metamielócito, mielocito e muito menos promielócito na diferencial.
Se aparecer o IG, e você não encontrar nenhuma dessas 3 células na diferencial, se preocupe em verificar sua coloração, local de análise e até mesmo seu conhecimento morfológico!
O IG é um marcador da “prateleira de cima” da hematologia, se você tem ele no seu equipamento, faça um informe para os médicos sobre os benefícios dele.
Entretanto a contagem de bastonete ainda é um índice mais precoce para processo inflamatório agudo!

A TALASSEMIA NEM SEMPRE E DIAGNOSTICADA
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
31/10/2023 |
 #Padronização
#Sindromes
#exames
#Padronização
#Sindromes
#exames
A TALASSEMIA EXISTE!
Sim, e ainda é responsável por uma boa parcela das ANEMIAS MICROCITICAS E HIPOCRÔMICAS!
Claro que a anemia ferropriva é a doença mais comum do mundo, mas preste atenção nisso:
Se você tiver uma anemia com microcitose e hipocromia (VCM e HCM), e os índices de ferro estiverem normais, NÃO SE TRATA de anemia ferropriva.
PESQUISE TALASSEMIA!
É uma anemia hereditária, com origem na região do mar mediterrâneo aonde o problema é a diminuição da síntese de uma das cadeias de globina.
Esse fator causa várias alterações (TODAS DISCUTIDAS NO HEMOCLASS LAN), e leva à um quadro hemolítico que pode ser leve, moderado ou intenso.
Pra te encurtar a conversa, o exame que vai identificar o diagnóstico de talassemia é a eletroforese de hemoglobina.
RESUMINDO: Se o paciente apresentar anemia microcítica e hipocrômica com níveis normais de ferro, o exame que você precisa sugerir ao médico é a eletroforese de hemoglobina.
Outro fator que contribui para a talassemia é uma anemia “desde sempre”, ou seja, o paciente sempre apresentou anemia, sempre fez uso de sulfato ferroso e nunca teve resultado.
Existem estados brasileiros que a prevalência de talassemia é bem considerável, então NÃO DESCARTE ESSA POSSIBILIDADE!
Aproveito e deixo o link de um artigo que fala sobre as hemoglobinopatias e suas frequências:
https://www.scielosp.org/article/rbepid/2019.v22suppl2/E190007.SUPL.2/




