 Blog HemoClass
Blog HemoClass
 TAG: #HemoClass Leucemias
TAG: #HemoClass Leucemias
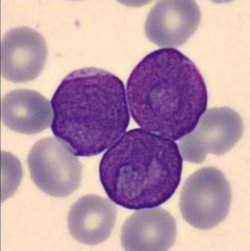
Blastos com Cup Like
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
23/06/2020 |
 #Leucemia
#Leucograma
#Hematoscopia
#Sindromes
#HemoClass Leucemias
#Leucemia
#Leucograma
#Hematoscopia
#Sindromes
#HemoClass Leucemias
Nas leucemias, uma microscopia bem feita pode ser a diferença entre um diagnóstico assertivo e precoce de uma evolução mais complicada por não se direcionar o quadro para o rumo correto. Algumas alterações morfológicas permitem uma sugestão diagnóstica, como no caso as faggot cells para Leucemia Promielocítica Aguda, os blastos linfoides vacuolizados para linfoma de Burkitt entre outros.
Também é possível, em algumas situações, a correlação morfológica com anormalidades genéticas.
Um achado morfológico importante nos blastos de leucemias agudas é invaginação nuclear proeminente, também chamado de blasto em forma de xícara, ou boca de peixe, ou simplesmente cup like.
Essa alteração morfológica resulta no acúmulo de organelas citoplasmáticas, devido à alterações de transporte do núcleo de NPM1, e nela já foi identificado, através de microscopia eletrônica, uma coleção de mitocôndrias dentro da bolsa nuclear invaginada, comprimindo parcialmente a cromatina.
A morfologia Cup Like está relacionadas com mutações proeminentes nos genes NMP1 e FLT3-ITD, com a ausência da expressão de CD34 e HLA-DR. Ainda se associa uma leucometria elevada com alta contagem de blastos no sangue periférico e na medula óssea, geralmente com cariótipo normal.
Sabe-se que a presença de mutações no gene FLT3 é de prognóstico desfavorável e que as mutações no gene NPM1 do tipo A são de prognóstico favorável, o que reforça a necessidade de se investigar essas mutações quando a morfologia cup like se faz presente.
Nos países desenvolvidos, a análise das mutações no gene FLT3 e NPM1 tem sido considerada como um fator de prognóstico importante na decisão terapêutica em pacientes com diagnóstico de leucemias mieloides agudas.
jpeg.jpg)
Tricoleucemia e seus achados
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
03/10/2019 |
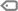 #Leucemia
#Hematoscopia
#Sindromes
#HemoClass Leucemias
#Leucemia
#Hematoscopia
#Sindromes
#HemoClass Leucemias
O relato de um laboratório do interior do estado do Paraná traz o seguinte:
Paciente 72 anos, masculino
Hemograma:
Eri: 2,21 / Hb: 7,6 / VG: 23,9 / VCM: 108,4 / HCM: 34,6 / CHCM: 31,9 / RDW: 21,1
Leucócitos: 3.200
Dif. Aparelho:
Linfo: 61,8 / Mono: 23,9 / Granulócitos: 14,3
Plaquetas: 22.000
A pancitopenia é observada no hemograma.
Diferencial manual:
Bt 2 / Seg 30 / Eosi 1 / Baso 0 / Linf 62 / Mono 4 / Reat 1
Ao se analisar a lâmina percebe-se vários linfócitos, com citoplasma com aspecto de franjas, que foram descritos como células linfoides variantes, com tamanho médio a grande, núcleo com cromatina densa, citoplasma levemente basofílico com franjas/projeções citoplasmáticas, sugestivo de tricoleucócitos.
A tricoleucemia é uma doença linfoproliferativa crônica de linfócitos B, e está relacionada com a exposição à radiação, benzeno, pesticidas e herbicidas, com incidência maior é em homens com idade entre 50 à 55 anos. Antigamente era conhecida como reticuloendoteliose leucêmica.
Clinicamente se observa sintomas relacionados com anemia, trombocitopenia e leucopenia, podendo ser cansaço, fadiga, fraqueza, além de sangramentos do tipo púrpura (petéquias, equimoses, epistaxe e gengivorragia), além de infecções de recorrência.
A forma pancitopênica prevalece, com 85% dos casos, mas ainda é possível se ter a forma leucêmica (15%), aonde se observa uma leucocitose com anemia e trombocitopenia. Ambas apresentam células cabeludas na extensão.
Nestas situações o acúmulo celular acontece pelo aumento da sobrevida das células e não pela proliferação como em leucemias agudas.
As células cabeludas, ou tricoleucócitos, são maiores que os linfócitos normais, com o citoplasma fracamente basófilo exibindo projeções citoplasmáticas. Em alguns casos ainda se observa granulações citoplasmáticas. O núcleo é excêntrico, arredondado ou oval. Uma prova confirmatória para essa situação é a coloração da Fosfatase Ácida Tartarato Resistente (FATR), que fica positiva em casos de tricoleucemia.
Os critérios de diagnóstico da TL são:
presença de pancitopenia,
presença de hairy cells no sangue periférico,
esplenomegalia (ocorre em 90% dos pacientes)
infecções de recorrência (devido a pancitopenia).
A prova citoquímica da FATR associada com os critérios acima é essencial para o diagnóstico.
O diagnóstico definitivo acaba acontecendo por biópsia de medula óssea e não por aspirado, uma vez que é comum a fibrose medular em casos de tricoleucemia.
O imunofenótipo do tricoleucócito é o de uma célula B madura: CD19, CD20, CD22 e CD79a, sendo que a expressão de CD22 é forte.
Corpos de Russell
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
01/10/2019 |
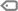 #Leucemia
#Leucograma
#Padronização
#Hematoscopia
#HemoClass Leucemias
#Leucemia
#Leucograma
#Padronização
#Hematoscopia
#HemoClass Leucemias
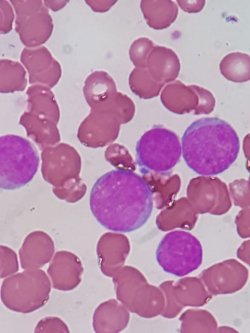
Os corpos de Russell são inclusões citoplasmáticas esféricas ou globulares eosinofílicas que se acumulam no retículo endoplasmático rugoso distendido das células plasmáticas maduras. Essas células plasmáticas contendo corpos de Russell também são conhecidas como células de Mott, e foram descritas pela primeira vez em 1890 por William Russell.
Trata-se de inclusões eosinofílicas, grandes e homogêneas, contendo imunoglobulina, geralmente encontradas em células plasmáticas submetidas a síntese excessiva de imunoglobulina.
Basicamente essa inclusão é observada na análise histopatológica da gastrite e também nas doenças de células plasmáticas como mieloma múltiplo, por exemplo.
A gastrite com corpúsculos de Russell , que pode estar associada à infecção por Helicobacter pylori, é uma lesão recentemente reconhecida que se caracteriza pela presença de inclusões eosinofílicas intracitoplasmáticas em plasmócitos.
Nas plasmocitoses, tanto reativas quanto neoplásicas, essas inclusões podem ser observadas, como inclusões hialinas redondas, presentes no citoplasma do plasmócito. Pode estar presente tanto na medula óssea quanto no sangue periférico.
Acúmulo se dá por desequilíbrio entre produção e degradação das proteínas celulares, causando perda da homeostase. Geralmente formam corpúsculos no interior da célula.
É importante que se relate no hemograma essa inclusão quando presente, seja de forma isolada (presença de corpos de Russell nos plasmócitos) ou na forma celular (presença de células de Mott).
Leucemia Mieloide Aguda M2 Caso Clinico
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
17/09/2019 |
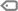 #Leucemia
#Sindromes
#exames
#HemoClass Leucemias
#Leucemia
#Sindromes
#exames
#HemoClass Leucemias
Leucemia Mielóide Aguda M2 (FAB) ou Leucemia Mielóide Aguda com translocação 8:21 (OMS)
Apresentação de Caso e Revisão Literária
Paciente com 64 anos, procura o médico com queixas de falta de apetite, cansaço e fraqueza.
Hemograma:
Eri: 3,23 / Hb: 9,2 / VG: 26 / VCM: 83 / HCM: 29,4 / CHCM: 35,4 / RDW: 13,5
Leucócitos totais: 67,4
Dif. Aparelho:
Linf. 33,7 / Mon. 27 / Gran: 39,3
Plaquetas: 81.000
Percebe-se claramente a tríade leucêmica ao analisar o hemograma. Os blastos não apresentam bastonetes de auer, entretanto mostram inclusões que lembram os corpos de PHI.
Pelas fotos percebe-se claramente a presença de blastos, e a contagem diferencial foi:
Blastos: 83% / Prómielócitos: 2% / segmentados: 2% / linfócitos: 12% / monócitos: 1%
As observações incluíram:
Blastos de tamanho pequeno à médio, com moderada relação N/C, crimatina frouxa e nucléolos evidentes, alguns com citoplasma granular e núcleos pleomórficos.
Após encaminhamento ao hematologista, o mielograma foi realizado:
O mielograma revelou uma medula óssea hipercelular, infiltrada por 68% de mieloblastos, com maturação granulocítica, representada por 16% de granulócitos parcialmente hipogranulares. Celularidade restante com 8% de eritroblastos, 2% de linfócitos e 6% de monócitos. Hipoplasia granulocítica, e ausência de parasitos e células estranhas à medula.
Os critérios diagnósticos descritos na literatura para LMA m2 são:
Blastos > que 30% das células da MO
Blastos entre 30 e 89% das células não eritróides da MO
Componente granulocítico em maturação > 10% das células não eritróides
Componente monocítico (monoblasto para monócito) <20% das céluas não-eritróides.
Ausência de critérios da m4
Com essa descrição a sugestividade diagnóstica ficou para LMA m2, devendo ser feita a imunofenotipagem para confirmação.
Revisão da LMA m2:
O mieloblasto se apresenta, na maioria das vezes dos casos de LMA m2, com uma cromatina porosa, um ou dois nucléolos, relação N/C diminuída e grânulos citoplasmáticos.
Geralmente os Bastonetes de auer são frequentes, o que não se observou nesse caso. Promielócitos, mielócitos e granulócitos maduros com variados graus de displasia são vistos na medula óssea, conforme o descrito no mielograma.
Os eritroblastos e megacariócitos são morfologicamente normais. A reação citoquímica para MPO é positiva em pelo menos 3% dos blastos, quando realizada.
Essa leucemia corresponde a 12% de todos os casos de LMA, sendo mais comum em crianças e adultos jovens. Ainda é comum se achar pseudo-chediak-higashi em uma variante da m2, e hipogranulia nos neutrófilos, conforme relatado.
Na imunofenotipagem os blastos apresentam os marcadores: MPO, CD13, CD33, CDw65, CD117, e a alteração genética característica é a translocação 8:21 (q22;q22)
Relevância clínica: A LMA-M2 t(8;21) tem maior taxa de remissão completa e possui melhor prognóstico em pacientes adultos; em crianças os estudos ainda são inconclusivos.
Existe uma variante da m2, que apresenta as seguintes características:
Blastos grandes, com frequente bastonete de auer e granulação abundante
Comum granulócitos imaturos com displasia (PM, MI, MT)
Pode aparecer pseudo-Pelger-Huet e Pseudo-Chediak-Higashi
Pode aparecer precursores eosinofílicos na MO e não em SP
Comum em pacientes com síndrome de Down
Marcadores extras: CD19 e CD56

Celulas Sugestivas
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
23/07/2019 |
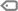 #Leucemia
#Leucograma
#Hematoscopia
#HemoClass Leucemias
#Leucemia
#Leucograma
#Hematoscopia
#HemoClass Leucemias
Na oncohematologia existem algumas alterações de hemograma ou células características que trazem consigo uma forte sugestão de uma ou outra patologia específica. Listamos algumas delas aqui.
1) Célula de Mott – Mieloma Múltiplo
2) Fagott Cell – LMA m3
3) Blastos em forma de Alteres – LMA m3V
4) Blastos com características monocitóides – LMA m4 e m5
5) Blastos basofílicos e vacuolizados – Linfoma de Burkit/LLA l3
6) Baskett Cell / Machas de Gumprecht – LLC
7) Blasto com Bastonete de Auer – LMA
8) Eritroblastos displásicos – SMD
9) Blastos com brotamentos – LMA m7 (mas pode aparecer em outras)
10) Célula em Espelho de Mão – Linfoma Leucemizado
11) Linfócitos pequenos com cromatina condensada (monotonia celular) – LLC
12) Flower Cell - Linfoma de célula T
Gostou desse artigo? Não deixe de comentar logo abaixo!!!
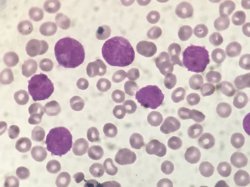
Leucemia Promielocitica Aguda variante Hipogranular
Warning: strtotime(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
Warning: date(): It is not safe to rely on the system's timezone settings. You are *required* to use the date.timezone setting or the date_default_timezone_set() function. In case you used any of those methods and you are still getting this warning, you most likely misspelled the timezone identifier. We selected the timezone 'UTC' for now, but please set date.timezone to select your timezone. in /home/hemocla/public_html/site/blog.php on line 179
14/05/2019 |
 #Leucemia
#Padronização
#Hematoscopia
#exames
#HemoClass Leucemias
#Leucemia
#Padronização
#Hematoscopia
#exames
#HemoClass Leucemias
A LPAv (Leucemia Promielocítica Aguda variante hipogranular), assim como a LPA, é uma neoplasia hematológica decorrente da translocação entre o cromossomo 15 e o cromossomo 17. Esta translocação faz acontecer um gene quimérico (PML - RARα), que expressa uma oncoproteína que é um receptor para o ácido retinóico, fazendo com que a célula mutada estacione na fase de pró-mielócito e perca sua capacidade de maturação, e aumente a sua capacidade de proliferação.
Leucopenia costuma ser frequente na LPA, com vários blastos granulares e também células com numerosos bastonetes de auer, chamadas de faggot cells. A leucopenia acontece pelo fato dos pró-mielócitos terem uma certa rigidez, e isso dificulta a sua saída da medula óssea. Esses pró-mielócitos anômalos acabam por ser ativadores da cascata da coagulação, quando fazem a liberação de sua granulação na corrente circulatória, fazendo CIVD logo no início da liberação das células para o sp, outro fator que explica a leucopenia, visto que assim que os pró-mielócitos começam a sair da medula óssea, a CIVD já acontece, levando o paciente à procurar o serviço de saúde.
Já na sua variante hipogranular, as células acabam tendo uma mobilidade maior, e a CIVD não é tão evidente quanto na LPA. Embora a causa e a fisiopatologia seja a mesma, este subtipo variante não apresenta tantas granulações e bastonetes de auer, embora os mesmos possam ser vistos em quantidades moderadas.
A variante hipogranular da LPA representa, em média, 4% dos casos das LMA (Leucemias Mielóides Agudas), acometendo principalmente adultos jovens.
No hemograma da LPAv, se espera encontrar a tríade leucêmica com leucocitose ou hiperleucocitose. Os blastos apresentam formato reiniforme, com aspecto semelhante a “asas de borboletas”, ou formato de alteres. Os bastonetes de auer geralmente são encontrados, e acabam facilitando a sugestão diagnóstica, juntamente com a morfologia dos blastos.
Em 2016, a OMS propôs uma nova classificação, e essas leucemias, que no grupo FAB correspondiam à LMA m3 e m3v, passaram a corresponder à um subtipo próprio, desvinculado das LMAs, sendo sugerido que se utilize a nomenclatura LPA e LPAv.
Saiba mais sobre este e todos os outros subtipos de leucemia no melhor treinamento online sobre Leucemia do Brasil!!!
Um curso que realmente vai te deixar afiado para encarar essas alterações morfológicas!!!
Agora o curso está com inscrições encerradas, mas muito em breve abrirá uma nova turma!!




